نقش دوگانهی پالادیم: همگن و ناهمگن در سنتز وینیلاستات
خلاصه
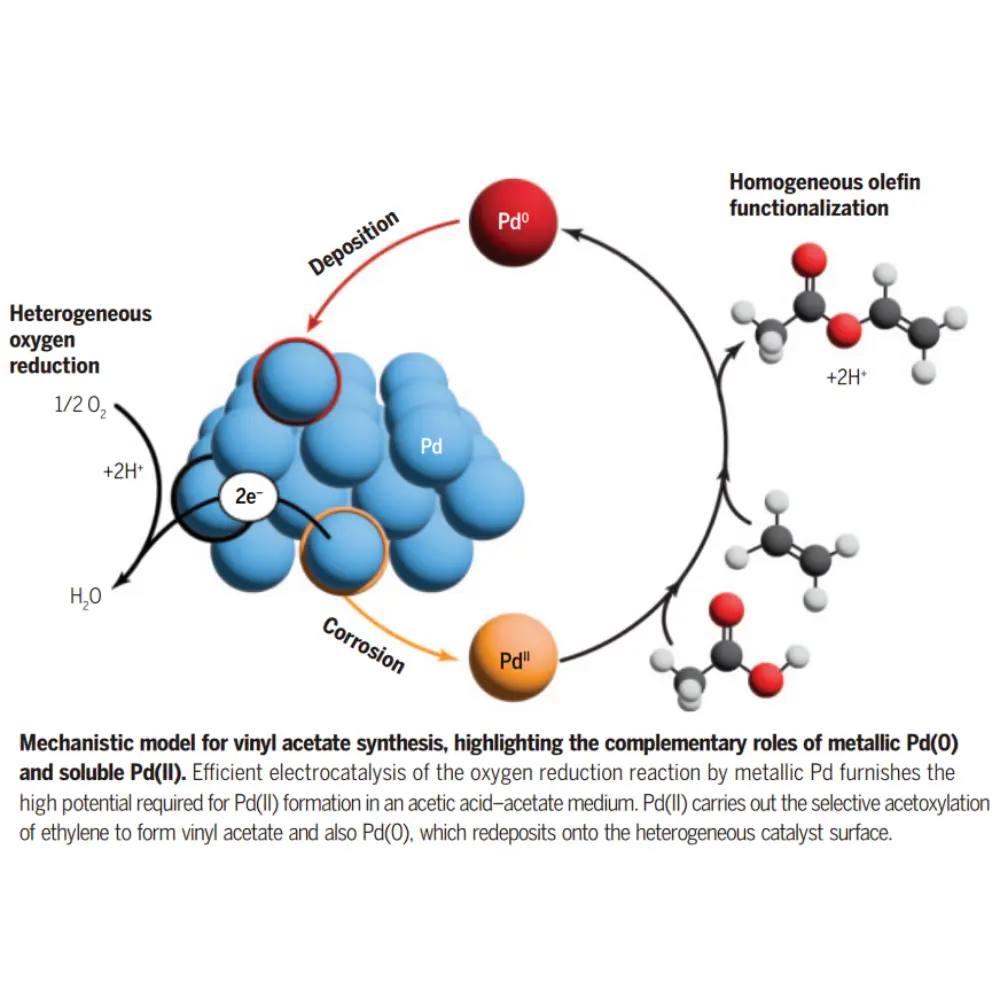
سنتز وینیلاستات یکی از فرایندهای صنعتی بزرگمقیاس است، اما نقش واقعی گونههای مختلف پالادیم—اعم از فلز نانولایهای در سطح کاتالیزور و گونههای محلول Pd(II)—برای دههها مبهم مانده بود. این مطالعه با بهرهگیری از الکتروشیمی نشان میدهد که تبدیل پویا میان دو فاز ناهمگن Pd(0) و همگن Pd(II) نهتنها رخ میدهد، بلکه برای پیشبرد چرخهی کاتالیزی ضروری است. در این سازوکار، هر فاز عملکرد مکملی دارد: Pd(0) بهعنوان الکتروکاتالیزور احیای اکسیژن و Pd(II) بهعنوان عامل اصلی استیلاسیون اتیلن عمل میکند. یافتهها نشان میدهند که در شرایط مایع و بخار، سرعت واکنش مستقیماً با پتانسیل الکتروشیمیایی کاتالیزور مقیاس میشود و توقف خوردگی Pd(0) چرخه کاتالیز را مختل میکند. این نتایج دیدگاه کلاسیکِ تفکیک کامل کاتالیز همگن و ناهمگن را به چالش میکشد.
مقدمه
اگرچه مدتهاست که این موضوع شناخته شده که مواد کاتالیزوری ناهمگن میتوانند بهعنوان پیشکاتالیزورهایی برای گونههای فعال همگن عمل کنند—و بالعکس—اما بهندرت پیش میآید که هر دو فاز در یک چرخهی کاتالیزی واحد فراخوانده شوند. تعیین فاز کاتالیزور، رویکردهای بعدی در مطالعهی علمی و طراحی عقلانی کاتالیزور را شکل میدهد. مسئلهی فاز کاتالیزور بهویژه برای سنتز وینیلاستات کاتالیزشده با پالادیم (Pd) که یک فرایند صنعتی بزرگمقیاس است، اهمیت ویژهای دارد.
در این واکنش، از کاتالیزورهای فلزی Pd ناهمگن استفاده میشود، و لایههای نازکی از اسید استیک بر سطح کاتالیزور تشکیل میگردد که امکان ایجاد گونههای محلول Pd(II) را فراهم میکند. سازوکار سنتز وینیلاستات همچنان بهخوبی شناخته نشده است، زیرا نقشهای Pd(0) ناهمگن و Pd(II) همگن نامشخص باقی ماندهاند.
در این پژوهش، ما از پروبهای الکتروشیمیایی برای بررسی سنتز وینیلاستات استفاده کردیم و نشان دادیم که تبدیل متقابل میان Pd(0) ناهمگن و Pd(II) همگن برای کاتالیز ضروری است و هر یک از این گونهها نقش مکملی در چرخهی کاتالیزی ایفا میکنند.
استدلال
ما این دیدگاه را مطرح کردیم که الکتروشیمی میتواند ابزار منحصربهفردی برای روشنسازی نقش Pd(II) در این واکنش فراهم کند، زیرا تشکیل Pd(II) از طریق خوردگی پالادیم فلزی صورت میگیرد—فرایندی که ذاتاً الکتروشیمیایی است. بنابراین، پتانسیل الکتروشیمیایی کاتالیزور و اینکه چگونه نرخ واکنش با این پتانسیل مقیاس میشود، نقش خوردگی را در چرخهی کاتالیزی روشن میکند.
ما آزمایشهای پتانسیومتری و ولتامتری را در یک الکترولیت اسید استیک–استات پتاسیم بهعنوان محیط واکنش مایعفاز مدل انجام دادیم و مطالعات خود را با توسعهی یک روش پتانسیومتری الکترولیت جامد، به شرایط مرتبطتر صنعتی در فاز بخار گسترش دادیم.
نتایج
در محیط مدل اسید استیک–استات پتاسیم، دریافتیم که Pd/C دچار خوردگی شده و استات Pd(II) را تشکیل میدهد؛ این فرایند توسط O₂ یا الکترولیز آندی پیش رانده میشود. در همین محلول، استات Pd(II) با سرعت زیاد با اتیلن واکنش داده و وینیلاستات را بهصورت انتخابپذیر تولید میکند و همزمان Pd(0) را دوباره ایجاد میکند.
در شرایط واکنش ترموشیمیایی، تغییر فشار جزئی O₂ همزمان هم نرخ تولید وینیلاستات و هم پتانسیل الکتروشیمیایی کاتالیزور Pd/C را تغییر میدهد. بر اساس این یافتهها، ما این فرضیه را مطرح کردیم که سنتز وینیلاستات میتواند از طریق خوردگی Pd(0) به Pd(II) با محرک O₂ یا با اعمال قطبش خارجی پیش رود، و سپس استیلاسیون سریع اتیلن بهواسطهی Pd(II) صورت گیرد.
ما مقیاسبندی نرخ پتانسیل را میان سه حالت مقایسه کردیم:
-
سنتز ترموشیمیایی هوازی وینیلاستات (با اندازهگیری پتانسیل مدار باز و نرخ واکنش حرارتی Pd/C در حضور اتیلن و مقادیر مختلف O₂)،
-
سنتز الکترولیتی وینیلاستات (از طریق قطبش خارجی Pd/C در حضور اتیلن و نبود O₂)،
-
خوردگی الکترولیتی (قطبش خارجی Pd/C در جو بیاثر)
هر سه فرایند، یک مقیاسبندی مشترک میان نرخ تشکیل محصول و پتانسیل کاتالیزور نشان دادند، که بیانگر این است که آنها یک گام انتقال بارِ مشترک و از نظر سینتیکی مرتبط را به اشتراک میگذارند که از نیمواکنش خوردگی Pd ناشی میشود.
این مشاهدات یک مدل مکانیکی برای سنتز ترموشیمیایی وینیلاستات را پشتیبانی میکنند که در آن Pd(0) نانوذرهای ناهمگن بهعنوان الکتروکاتالیزور فعال احیای اکسیژن عمل میکند و پتانسیلهای بالای لازم برای خوردگی و تشکیل Pd(II) همگن را فراهم میکند. گونهی Pd(II) حاصل، سپس استیلاسیون انتخابپذیر اتیلن را انجام داده و دوباره بهصورت Pd(0) ناهمگن رسوب میکند.
برای گسترش این بررسی مکانیکی به فاز بخار، ما از پتانسیومتری الکترولیت جامد با الکترولیت حالت جامد سدیم β″-آلومینا استفاده کردیم تا پتانسیل کاتالیزور را بدون حضور فاز مایع تعیین کنیم. در شرایط واکنش فاز بخار نیز همان الگوی نرخ–پتانسیل مشاهده شد که در واکنش مایعفاز دیده شده بود، و این نشان میدهد که یک سازوکار مشابه در فاز بخار نیز فعال است.
علاوه بر این، مهار خوردگی Pd(0) به Pd(II) از طریق حفاظت گالوانیکی موجب غیرفعالسازی برگشتپذیر کاتالیز در هر دو فاز مایع و بخار شد، که اهمیت حیاتی تبدیل فازی را در این چرخهی کاتالیزی برجسته میکند.
نتیجهگیری
نتایج ما به سازوکاری اشاره میکنند که در آن تبدیل فاز کاتالیزور یک فرایند مسیر–وابسته (on-pathway) است و برای ایجاد یک سیستم کاتالیزی دوکارکردی ضروری است؛ سیستمی که در آن Pd(0) ناهمگن و Pd(II) همگن بهترتیب نقشهای مکمل احیای اکسیژن و تابعدارکردن الیفن را بر عهده دارند.
این الگو، فرض ضمنی رایج را که کاتالیز یا بهصورت کاملاً همگن یا کاملاً ناهمگن صورت میگیرد به چالش میکشد و نشان میدهد که تبدیل پویا میان فازهای مولکولی و مواد میتواند واکنشپذیری مکمل را ترکیب و تقویت کند.
منابع و توضیحات:
Deiaa M. Harraz et al.,Homogeneous-heterogeneous bifunctionality in Pd-catalyzed vinyl acetate synthesis.Science388,eads7913(2025).DOI:10.1126/science.ads7913